オゾン・紫外線殺菌の概要
オゾン殺菌について
あらゆる方面に効果の期待が高まる紫外線殺菌灯
安全で殺菌力の強い波長253.7nmと、強力な酸化作用と消臭効果を持つオゾン の発生を伴う波長184.9nmとの組み合わせにより、あらゆる場面において優れた効果を発揮します。
オゾンの発見について

オゾンは、1840年にドイツ・スイスの化学者で、ニトロセルロースの発見者として有名なクリスチアン・フリードリヒ・シェーンバイン(Christian Friedrich Schönbein、1799年 – 1868年) によって発見されました。
1838年、燃料電池の原理を発見、1939年にはオゾンが酸素から成り立っている事を緩慢な白燐の酸化と水の電気分解の実験中に発見しました。 これらの実験はシェーンバインがスイスのバーゼル大学の教授に就任した1928年より、特有の臭気に気を留めた事をきっかけに’始まりました。
オゾンは奇妙な臭いを放ちます。同じような匂いが雷雨にも生じる事をきっかけとしてオゾンは大気からできると推測しました。シェーンバインは彼の実験装置で実証し、この強い臭いからギリシャ語の「臭い」を意味する“ozein”から“OZON(オゾン)”と名づけられました。
彼の一連の発見と研究を記した論文は『ある化学反応に起因する臭気の性質』として1840年、パリでフランス科学アカデミー誌に掲載されました。
地球のオゾンと紫外線とは
私たちの住む地球は太古の昔から太陽の恩恵を限りなく受けています。
その太陽から電磁波の一種、紫外線が広範囲にわたり放射されています。紫外線の中でも300nm以下の短波長の光は高いエネルギーを持ち、生物を死滅させてしまう危険な光です。
しかし、オゾン層によって、その光は吸収され、私たちの住む地球上には幸いなことに届きません。オゾン層破壊が問題となるのはそのためです。
一方で、紫外線は、それを有効に利用することにより、住み良い環境を提供してくれています
紫外線の殺菌作用やオゾンの生成作用などを活用することで、生物が生きていくために必要な空気や水の浄化に利用できる環境を可能としてくれています。
オゾン特性
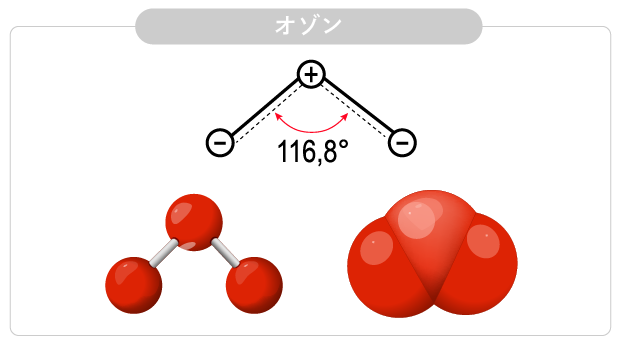
オゾンは酸素(O2)の同素体(同一種類の元素で出来ているのに構造が互いに異なる物質を
同素体と言います)で、分子記号はO3、分子量は48、沸点-112℃ 、融点-193℃、臨界温度-12℃、比重は空気の1.54倍、酸素の3倍と重いですが、塩素よりは軽いものです。水への溶解度は酸素の約10倍と高い溶解度です。除菌力は 天然元素の中ではフッ素に次いで高く、空気中では塩素の約1.65倍、水中では約7倍と言われています。
オゾン(O3)は非常に不安定な気体であるため、生成されたオゾンは常温で徐々に分解して、安定した酸素()2)になります。
第三の原子(O)の結合がゆるいために、容易に1原子の酸素(O)を放出するので、酸化力が強く、有機物、無機物を酸化します。
また、微生物(細菌、真菌など)、臭気物質にも作用して、除菌、脱臭、色素類の脱色もします。
オゾンは、通常の反応によって、毒性のある副次物を生成しないことから二次公害の心配がないこと、原料は空気または酸素であるので、どのような場所でも随時任意の量が得られることなどの利点があり、近年は高濃度オゾン発生装置の開発により上・下水処理、食品製造工程での除菌・脱臭、食品の原材料の処理、貯蔵に利用されるようになってきております。
オゾンの発生方法
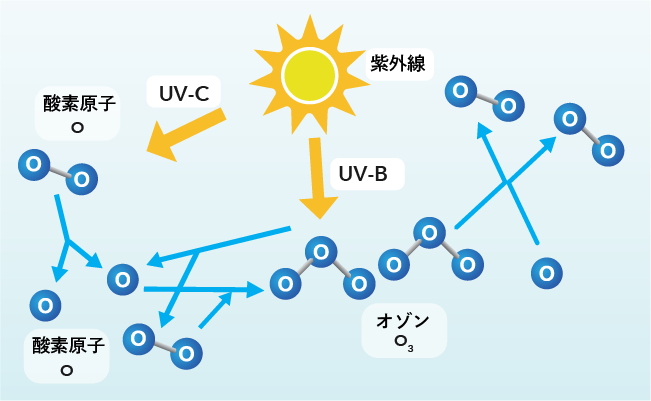
先にオゾンは紫外線や雷の放電によって生成されると述べましたように、オゾンを発生させる方法にはいくつかの方法がありますが、主な方法には次のものがあります。
光化学反応法
この方法は、オゾン層におけるオゾン生成のメカニズムと同じ原理です。つまり、紫外線の中でも更に波長の短いオゾン発生線とよばれる光線を酸素分子(O2)に照射すると、酸素分子(O2)が解離して酸素原子(O)が2個生じます。この酸素原子(O)が他の酸素分子(O2)と結合してオゾン(O3)が生成されるのです。
O2+O=O3
一般に紫外線によるオゾンの生成には紫外線ランプが使用されますが、この方法の特徴として、紫外線の中にはオゾンを生成する波長の光線と、オゾンを分解する波長の光線があるために、同時にオゾン、O⁻、OHラジカルの3種類の物の生成と分解の反応が並列して起こること、さらに分解反応で生じた酸素原子(O)がオゾンと反応してオゾンを壊すという現象が起こるために、あまり高濃度なオゾン発生は期待できないと言われています、故に紫外線ランプ式は発生量と室内容積を最適に計算すれば24時間使用と安全性を両立させる事も可能になります、また分解で生じた(O)が空気中の水蒸気と反応しOHラジカルを作ります、このOHラジカルが即座に近くの臭い物質や細菌、ウィルス類を低温燃焼させます。
低濃度オゾンにもかかわらず除菌、脱臭効果が高いのもこの紫外線とオゾンで作るO⁻、OHラジカルの分解力がオゾンの効果にプラスされるためです。
※1:O⁻
活性酸素のこと オゾンに紫外線(254nm)照射->O2+O⁻。
※2:OHラジカル 周囲にオゾンと紫外線(254nm)と高湿度がある環境の場合発生しやすい。
通常、電子は一つの軌道に2個づつ対をなして収容されますが、何らかの原因(あるいは操作)で、一つの軌道に電子が一個しか存在 しないことがあります。このような「不対電子」を持つ原子または分子をフリーラジカル(遊離活性基)と言います。酸素(O)と水素(H)原子それぞれ1個が結合したOHがフリーラジカルの状態にある場合、これをOHラジカルと言います。
本来、電子は軌道で対をなっている時がエネルギー的に最も安定した状態ですので、フリーラジカルは他の分子から電子を取って、安定になろうとします(ある原子や分子から電子が一個なくなることを、その物質は「酸化」されたと言います)。つまり、フリーラジカルは相手の物質を酸化する力が強い分子です。例えば、OHラジカルのダイオキシンに対する反応速度はオゾンの109~1010倍と報告されています。
なお、O⁻、OHラジカル自身は非常に寿命が短いため、空気中に混入したまま環境に出て人体や生態系に影響を与えるというようなことはありません。
殺菌のメカニズムについて
オゾンはフッ素に次ぐ強力な酸化作用があります。
殺菌・ウイルスの不活化・脱臭・脱色・有機物の除去などに用いられます。
オゾンは活性の高い酸素を含む化学種であり、広い意味で活性酸素の一つとされます。
身体に害があるとして話題になった「活性酸素」は、スーパーオキシドアニオンラジカルやヒドロキシルラジカルを指します。水中では、オゾンの一部がヒドロキシラジカルを発生させます。
また、それだけでなく、オゾンと細菌体内の水分子と結合してヒドロキシルラジカル(OHラジカル)を発生することもあります。
ヒドロキシルラジカル (hydroxyl radical) はヒドロキシ基(水酸基)に対応するラジカルで、OH と表されます。
活性酸素と呼ばれる分子のなかでは最も反応性が高く、最も酸化力が強く、細菌の糖質やタンパク質や脂質などあらゆる物質と反応して分解して殺菌します。
しかし、その反応性の高さゆえ通常の環境下では長時間存在することはできず、生成後速やかに消滅します。
CT値とは
CT 値 ( Concentration-Time Value )は、殺虫・殺菌効果を表す評価指標で、ガス濃度を示すConcentrationと、時間を示すTimeの頭文字であり、ガス濃度と接触時間の積(ミリグラム/リットル×時間)を表しています。
殺虫・殺菌効果は、害虫・殺菌がどの程度のガス濃度にどのくらいの時間接触されるかによって決まるため、CT値が高いほど殺虫・殺菌効果は増加し、CT値が低いほど殺虫・殺菌効果は低下します。
ラジカルとは
ラジカル(radical)とは、不対電子を持つ原子や分子を指します。通常は 2個1組で軌道上を回転しているはずの電子が何らかの条件によって 1つしかなくなっている状態のことです。
ラジカルな原子は、電気的に非常に不安的で、周りの原子や分子から欠けた電子を奪おうとするために、極めて反応性が強い性質を持っています。
不安定で反応性に富む短寿命の中間体なので、かなりの速さで他の非ラジカル種と結合をして元の化合物を分解し、別の化合物を生成します。
細菌の体内の糖質やタンパク質や脂質などあらゆる物質と反応して、細菌の体を分解します。
紫外線について
人間の目に見える光の中で最も波長の短いものが紫色です。紫色より短い波長の光を紫外線と言います。
紫外線は波長の種類によって異なった性質があり、それぞれが重要な働きがあります。その中で、
250nm~260nm(ナノメーター)の紫外線に強力な除菌効果があります。
UVランプからは以下の2種類の紫外線が主に発生しております。
185nmの紫外線は酸素を解離するためにオゾンの生成に寄与する効果
254nmの紫外線はオゾンの分解とO⁻、OHラジカルの生成に作用します。

nm(ナノメーター)は、1兆分の1mです。因みに千分の1mは1mm(ミリメーター)、百万分の1mは1μm(マイクロメーター)です。
放電によって発生させる方法
放電によってオゾンを発生させる方法としては、無声放電方式によるもの、コロナ放電方式によるもの、またはいくつかの放電方式を組み合わせた複合放電方式がありますがそれぞれ発生方式の違いがあっても放電式である限り、必ず窒素酸化物(NOx)が発生します、この方式は定期的な清掃と、窒素酸化物(NOx)吸収、分解フィルタ-の交換が必要です、そうでないと発生オゾン濃度よりも数倍の窒素酸化物(NOx)を発生するようになることもあります。
紫外線殺菌の利点
殺菌力
紫外線は殺菌消毒効果が高く、特に波長260nm付近は直射日光の波長350nmの1600倍にも達し「ウイルス」から「かび」まですべての微生物を短時間で殺菌することができます。
安全性
殺菌後の毒物の残留がなく、使用する紫外線は透過力が非常に弱いためポリエチレン以外はほとんど透過しません。直接肉眼で短時間でものぞいたり、肌に直接照射しないで下さい。
オゾンの用途
脱臭・脱色・環境改善
脱臭を目的として、オゾン、O⁻、OHラジカルは食品関係ばかりでなく、下水道、し尿処理、浴室、病院、老人施設、畜産、水産関係などでも利用されています。オゾン、O⁻、OHラジカルによる脱臭は、悪臭成分の酸化分解と、オゾンの臭気成分との中和作用によって脱臭します。
臭いの成分が何であるかによってオゾン、O⁻、OHラジカルで脱臭できるかどうかが決定されますが、食品工場などで発生する臭いは微生物に由来するものが多いので、除菌と脱臭が同時に行われる場合もあります。オゾンは一般に、-SH、=S、-NH2、=NH、N、-OH、-CHO基を有する化合物との反応性が大きく、臭気成分の多くはこれらの基を持つためにオゾン、O⁻、OHラジカルによる脱臭が効果的なのです。なお、脱臭には、水中の臭気物質を除去する場合と大気中の臭気成分を除去する場合があります
除菌・減菌
微生物に対するOHラジカル・オゾン、O⁻、OHラジカルの除菌作用は次のように言われています。
- オゾン、O⁻、OHラジカルが細胞壁または細胞膜に作用し、次いで脂質の二重結合に反応が生まれ、細胞が分解される。
- 微生物細胞の表面にオゾン、O⁻、OHラジカルが作用する。
- 微生物酵素が酸化する。
- 細胞壁にオゾン、O⁻、OHラジカルが作用し、細胞透過率に変化が生じ、細胞が分解する。
また、オゾン、O⁻、OHラジカル除菌の特徴とは、
- 栄養細胞は比較的簡単に除菌できるが、胞子形成菌はより抵抗性を持っている。
- 好気性胞子形成菌の方が嫌気性胞子形成菌よりもより容易に除菌される。
- 気中や水溶液中の微生物に対する除菌効率は、接触時間、濃度、水温、PH、無機物および有機物の在量に著しく影響される。
などです。
オゾン、O⁻、OHラジカルによる除菌は、簡単に言えば溶菌といわれ、塩素が細菌の細胞壁を通して拡散し、酵素を侵し、結果として死滅させる作用とは異なり、細菌の細胞壁の破裂、又は分解によるものなのです、別に低温燃焼とも言われています。
水中でのオゾンによる細菌の除菌についての実験報告が多く発表されています。例えば大腸菌の場合、塩素では濃度0.1~0.2mg/Lで不活性化するのに対し、オゾンでは0.02~0.04mg/Lで不活性化すると言われています。このことは、オゾンは塩素の約1/10程度の低濃度でも有効であることを示しています。
また、O157大腸菌、ブドウ球菌、サルモネラ菌などについても同様な結果が得られます。
病原性細菌に対するオゾンの除菌の例
| 病原性細胞の種類 | オゾン濃度(ppm) | PH等 | 温度 (℃) | 作用時間 (分) | 死減率 (%) | 気・液 |
| 霊菌 | 0.6 | 寒天平板塗末法 | 13 | 60 | 100 | 気 |
| 大腸菌 | 0.6 | 寒天平板塗末法 | 13 | 30 | 100 | 気 |
| 尋常変形菌 | 0.6 | 寒天平板塗末法 | 13 | 15 | 100 | 気 |
| ネズミチフス菌 | 0.6 | 寒天平板塗末法 | 13 | 60 | 100 | 気 |
| 緑膿菌 | 0.6 | 寒天平板塗末法 | 13 | 60 | 100 | 気 |
| 蛍光菌 | 0.6 | 寒天平板塗末法 | 13 | 60 | 100 | 気 |
| 大腸菌 | 0.5 | 紙塗末法 | 5 | 60 | 100 | 気 |
| 大腸菌 | 0.5 | 紙塗末法 | 5 | 30 | 100 | 気 |
| 大腸菌 | 0.5 | 紙塗末法 | 5 | 10 | 100 | 気 |
オゾンの利用と効果
オゾンはその除菌・脱臭・脱色などの効果から、種々の分野でこれの利用と効果が期待されています。
| 利用場所 | 期待される利用効果 |
| 病院 | 医者・看護婦・患者の手洗い場、共同トイレ、浴室の除菌。病室、汚物処理、 ゴミ置き場の脱臭、病院内二次感染の予防。 |
| 会議室 | タバコ、体臭の脱臭。 |
| ホテル客室 | 客室、廊下、ロビーの脱臭。 |
| 飲食店 | トイレの脱臭。厨房、ストックヤードの除菌。食材のオゾン水洗浄状による除菌。 |
| ペットショップ | 店内の脱臭、除菌によるペットの病害の防止。 |
| カラオケBOX | BOX内の脱臭。マイクの除菌。 |
| 食品加工工場 | 加工工場の除菌、脱臭。冷蔵庫の除菌、脱臭。加工食品のオゾン水洗浄による除菌。 |
| スーパー | バックヤードの脱臭、除菌。 |
| 活魚水槽 | 養殖場でのオゾン水循環による病害発生防止。 |
| 老人ホーム | 居室の除菌、脱臭。浴室湯の循環浄化、脱臭。 |
オゾンの人体への影響
オゾンは、その生成過程で毒性のある二次生成物を生成せず、安全性の高い気体ですが、濃度が極めて高い場合には、強い毒性を示します。これは、オゾンが強い酸化力を持ち、反応性が高いためです。
また、水分に吸収されにくいので、呼吸器系に取り込まれた場合には肺の深部にまで到達して、呼吸器障害(肺水腫等)を引き起こすことが報告されています。通産省や労働省ではまだ確たる使用基準を定めていませんが、日本産業衛生学会:許容濃度委員会や、中央労働災害防止協会は0.1ppmを労働環境における抑制濃度と規定しています。
また、ACGIH(米国労働衛生専門官会議)では、8時間労働における許容濃度を同じく0.1ppmとし、15分以下の短時間曝露の許容濃度を0.3ppmと規定しています。
オゾンの人体に対する影響
| オゾン濃度(ppm) | 影響・作用等 |
|---|---|
| 0.01〜0.02 | 臭気を感じる(やがて慣れる)。 |
| 0.1 | 強い臭気、鼻・のどに刺激を感じる。 |
| 0.2〜0.5 | 3~6時間で視覚低下の症状が出る。 |
| 0.5 | 明らかに上部気道に刺激を感じる。 |
| 1〜2 | 2時間で頭痛、胸部痛、上部気道の渇きと咳が起こる。 曝露をくり返すと慢性中毒になる。 |
| 5〜10 | 脈拍増加、肺水腫の症状がでる。 |
| 15〜20 | 小動物は2時間以内に死亡する。 |
| 50 | 人間も1時間で生命が危険になる。 |
「オゾン処理報告書」 日本水道協会 昭和59年8月 40頁より
※実際にオゾンを取り扱う場合、幸いなことにオゾンが毒性を発揮する濃度では強烈な臭いがするため、不本意にその危険状態に長時間さら曝される危険性は極めて少ないと言われています。
これまで除菌に必要なオゾン濃度や人体に影響を与えるオゾン濃度などを表わす場合に、すべてppmという単位で述べてきました。これは容量濃度と呼ばれるもので、ppmとはpartspermillionの略で百万分率を表します。つまり、ある量が全体の百万分の幾つを占めるかを表し、主として体積に用いられます。
・室内の気温を20℃とした場合
容量濃度(ppm)=1.0×(20+273)/273×22.4/48=0.5ppmとなります。
これは1.0,m×1.0m×1.0m=1.0m3の容積に1.0mgのオゾンを入れると0.5ppmの濃度になるということです。
※人体が安全に作業できるオゾン濃度の上限は0.1ppmですから、オゾンの質量濃度は、この1/5の0.2mg/m3ということになります。
オゾン発生量を10mg/hr、10坪(33m2)の部屋で高さ3mとして約100m3、計算上オゾン濃度は0.05ppmになります。
実際には、オゾンの半減期、空気の換気回数、処理対象との反応スピードなどを考慮して、オゾン量を決めます。
除菌に要するオゾン量のシステムの安全率を決めるのは、建物の構造、気温、湿度、換気回数、室内空気の循環方法など多くの要素が絡みますので、注意が必要です。
一般的なオゾン利用の利点と難点
オゾン利用の利点
- オゾンは天然自然物である。
- 微生物に対するスペクトルが広く、かつ強力である。
- 耐菌性をつくらない。
- 余分に用いても自然に分解して無害な酸素になる。
- 生成物は酸化物で新規の毒性がない。
- 反応が表面に限定され内部を変質させない
- 塩素やホルマリンのような臭気が残らない。
- 紫外線と比較し除菌と同時に脱臭、漂白作用がある。
- 発生量、濃度の制御が容易で、取扱い上安全である。
- 環境への負荷が小さい。
オゾン利用の難点
- 製造コストが高い。
- 分解が早く、持続性がない。
- 内部への浸透性がない。
- 再増殖がある。
- 水への溶解度が低い。(溶解度は酸素の10倍程度)
- 溶質との反応が除菌速度より速い場合がある
他の殺菌法と比べて
紫外線殺菌
- あらゆる菌種に有効である。
- 対象物を変質させる心配がない。
- コンパクトな設備。
- 維持費が安価。
- 二次処理の必要がないため、工程の簡素化、時間短縮、経費節減が図れる。
- 常温で殺菌できる。
- 耐久菌を作らない。
他の殺菌方法の問題点
①熱殺菌
- 殺菌対象物を変質させる
- 殺菌対象物を変質させることがある。
- エネルギーコストが高い。
- 冷却工程が必要なため、細菌が付着しやすい。
- 耐熱性菌には適さない。
②薬品による殺菌
- 残留性がある。
- 二次処理が必要である。
- エネルギーコストが高い。
- 耐性菌を発生させることがある。
③フィルター除菌
- 交換頻度が要求される。
- ランニングコストが高い
このように様々な殺菌方法がとられる中で、紫外線殺菌は効力や経済性の面で 非常に優れており、幅広い要請にお応えできるこれからの殺菌法です。
またオゾンは強い酸化力により有害物質を分解し、バクテリアを殺菌します。 しかもオゾンは条件により異なりますが、数分~数時間で自然分解するため、塩素による殺菌のように残留による影響を与えません。
各種の微生物を死滅させるのに必要な殺菌線量
| 菌類 | 培地上の菌を99%%殺すのに 必要な照射量 (mW・sec/cm2) | |
| グラム陰性菌 | Proteus vulgaris Hau. 変形菌 Shigella dysenteriae 赤痢菌(志賀菌) Shigella paradysenteriae 赤痢菌(駒込BⅢ菌) eberthella typhosa チフス菌 Escherichia coli communis 大腸菌 Vibrio cholerae コレラ菌 Pseudomonas aeruginosa 緑膿菌 S.typhimurium サルモネラ菌 | 3.8 4.3 4.4 4.5 5.4 6.5 10.5 15.2 |
| グラム陽性菌 | Streptococcus hemolyticus 溶血連球菌(A郡) (Group A-Gr.13) Staphylococcus albus 白色ブドウ球菌 Staphylococcus aureus 黄色ブドウ球菌 Streptococcus hemolyticus 溶血連球菌(D郡) (Group D, C-6-D) Streptococcus faecalis R. 陽球菌 Mycobacterium tuberculosis 結核菌 Bacillus mesentericus fuscus 馬鈴薯菌 Bacillus mesentericus fuscus 馬鈴薯菌(芽胞) (spores) Bacillus subtilis 枯草菌 Bacillus subtilis (spores) 枯草菌(芽胞) | 7.5 9.1 9.3 10.6 14.9 10 18 28.1 21.6 33.3 |
| 酵母 | Bakers Yeast パン酵母 Saccharomyces ellipsoideus ブドウ酒酵母 Saccharomyces cerevisiae ビール酵母 untergar. Munchen Saccharomyces Sake 日本酒酵母 Zygosaccharomyces Barkeri 生姜酒ロウ Willia anomala ウイリア属酵母 Pichia miyagi ピチア属酵母 | 8.8 13.2 18.9 19.6 21.1 37.8 38.4 |
| 菌類 | 培地上の菌を99%%殺すのに 必要な照射量 (mW・sec/cm2) | |
| かび | Oospora lactis Mucor racemosus Penicillium roqueforti Penicillium expansum Penicillium digitatum Aspergillus glaucus Aspergillus flavus Aspergillus niger Rhizopus nigricans | 10.2 35.4 26.4 22.2 88.2 88.2 120 264 222 |
| ウイルス | Poliovirus-Polimyelitus Bacteriophage (E.coli) Influenza Infection Heptitus Tobaacco mosaic | 6 6.6 6.6 8 440 |
| 原生動物 | Chlorella vularis(Algas) Nemat ode eggs param ecium | 22 92 200 |